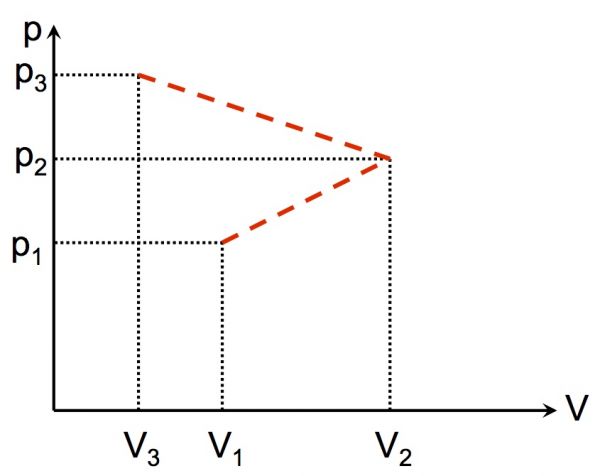
3,00 moli di gas ideale si trovano inizialmente allo stato 1 con pressione p1=20,0bar e volume V1=1500cm3. Passano allo stato 2 con pressione p2=1,50p1 e volume V2=2,00V1. Poi allo stato 3 con pressione p3=2,00p1 e volume V3=0,500V1. Calcolare la temperatura del gas negli stati 1 e 2. Qual è la variazione complessiva di energia interna dallo stato 1 allo stato 3?
Risoluzione
Utilizzando l’equazione di stato dei gas ello stato 1 si ha:
[{{rm{p}}_{rm{1}}}{{rm{V}}_{rm{1}}} = {rm{nR}}{{rm{T}}_{rm{1}}} Rightarrow {{rm{T}}_{rm{1}}} = frac{{{{rm{p}}_{rm{1}}}{{rm{V}}_{rm{1}}}}}{{{rm{nR}}}} = {rm{120K}}]
Nello stato 2 si ha:
[{{rm{p}}_{rm{2}}}{{rm{V}}_{rm{2}}} = {rm{nR}}{{rm{T}}_{rm{2}}} Rightarrow {{rm{T}}_{rm{2}}} = frac{{{{rm{p}}_{rm{2}}}{{rm{V}}_{rm{2}}}}}{{{rm{nR}}}} = {rm{361K}}]
Nello stato 3, infine, si ha:
[{{rm{p}}_{rm{3}}}{{rm{V}}_{rm{3}}} = {rm{nR}}{{rm{T}}_{rm{3}}} Rightarrow {{rm{T}}_{rm{3}}} = frac{{{{rm{p}}_{rm{3}}}{{rm{V}}_{rm{3}}}}}{{{rm{nR}}}} = {rm{120K}} = {{rm{T}}_{rm{1}}}]
Poichè T3=T1 l’energia interna dello stato 3 è uguale all’energia interna dello stato 1. Pertanto ΔEint,13=0